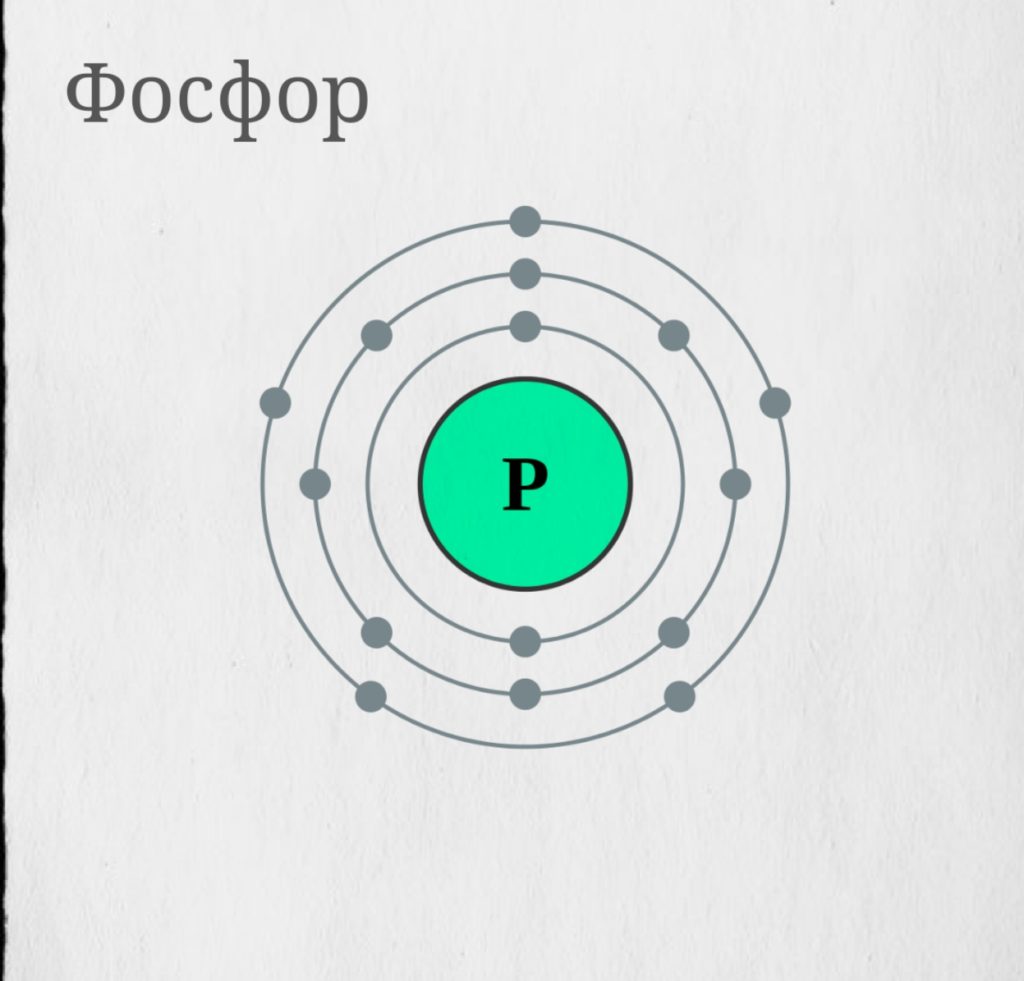
 Ф Фосфор является химическим элементом таблицы Менделеева с атомным номером 15 и обозначением P. Фосфор из-за его высокой реакционной способности в свободном виде в природе не встречается, а существует только в виде аллотропов.
Ф Фосфор является химическим элементом таблицы Менделеева с атомным номером 15 и обозначением P. Фосфор из-за его высокой реакционной способности в свободном виде в природе не встречается, а существует только в виде аллотропов.
Как был открыт Фосфор

История открытия фосфора является очень интересной. Вообще, кандидатов на открытие фосфора было очень много, так как несколько ученых объявили об открытии приблизительно одновременно. Само открытие было сделано 1669 году немецким алхимиком Хеннигом Брандом. Его желание создать легендарный «филосовский камень» и позволило свершиться этому открытию. Он ставил опыты над мочой в надежде из нее получить золото. Его предположение основывалось на том, что и то и другое одного цвета. Бранд держал мочу несколько дней пока та не начала издавать ужасный запах. После этого он сварил ее в пасту и нагрел до высокой температуры. Образовавшиеся пары он проводил через воду в надежде, что они сконденсируют в золото. Вместо этого он получил белое воскообразное вещество, которое светилось в темноте. Вот таким способом был открыт новый химический элемент.
Кстате, фосфор действительно является первым химическим элементом, который был по настоящему открыт. То есть об этом элементе не было известно вообще ничего и ни о каких его формах.
Где и как добывают Фосфор

Фосфор как отдельный химический элемент получают из фосфатных минералов, таких как фосфорит или апатит. Распространенность этих минералов довольно широкая. Ими в достаточных количествах обладают Россия, Китай, Индия, Канада, Бразилия и многие другие страны.
Получают элементарный фосфор нагревом фосфорита или апатита с кварцевым гравием при температуре около 1500°C. Необходимым условием является то, чтобы печь была выполнена в виде закрытой шахтной печи. Тепло должно передаваться через электроды Содерберга. Углеродная масса, содержащаяся в электроде действует как восстановитель, а диоксид кремния в этом случае служит в качестве генератора шлака. Газообразный фосфор конденсируется и собирается под водой в результате химичнских реакций.
Распространенность Фосфора

Распространенность фосфора является не полностью определенной. О распространенности фосфора во вселенной известно довольно немного. В 2013 году ученые выдвинули предположение, что фосфор в больших количествах вырабатывается при появлении сверхновых звезд. Не понятно из каких соображений сделаны такие выводы, но факт такого открытия присутствует.
Что касается Земли, то тут можно заметить, что ученые оценивают отношение содержания фосфора в земной коре как один грамм на один килограмм массы. В свободном виде из-за его высокой реакционной способности фосфор не встречается. Основные формы фосфора на Земле в виде соединений в минералах. К самым коммерчески важным относят апатит, вавеллит, вивианит и бирюзовый. На сегодняшний день дефицита фосфора не предвещается, но предположительно запасов хватит только на 400 лет.
Так же фосфор содержится в помете некоторых животных и птиц. В основном это касается морских животных и птиц. В пример можно привести гуано, которое является пометом птиц. Они могут содержать от 7 до 60% фосфатных соединений. Эти птицы были завиксированны на небольших островах принадлежащих современным Перу и Чили. Это свидетельствует о том, что океан является безграничным неизведанным запасом фосфора. Ежегодная добыча фосфоросодержащих минералов оценивается приблизительно в 180 миллионов.
Применение Фосфора

Что касается применения фосфора, то тут можно явно отметить, что на сегодняшний день оно является не очень широким. Сегодня 80% из 180 млн тонн добываемых фосфоросодержащих минералов перерабатывается до оксида фосфора(V), который является важнейшим сырьем для производства удобрений и различного рода средств защиты для растений. Таким образом большая часть переходит в пользование химической прлмышленности. Оставшаяся часиь фосфора тратится на металлургию, пищевую промышленность, медицину, изготовление фарфора и военное дело.
В металлургии фосфор применяется при производстве стали и фосфористой бронзы в качестве присадок. При изготовлении фарфора используется костная зола и фосфат кальция. В пищевой промышленности в качестве добавок используется фосфорная кислота изготовленная из чистого фосфора. Белый фосфор применяется в военной промышленности в качестве боевой части некоторых видов боеприпасов. В числе таких боеприпасов находятся зажигательные бомбы и снаряды. На сегодняшний день использование белого фосфора ограничено международным правом из-за его токсичности. Что касается медицины, то тут можно отметить, что используется именно радиоактивные изотопы фосфора в качестве индикатора при биохимических исследованиях.
Интересные факты

Интересных фактов связанных с фосфором достаточно много. Стоит начать с того, что потенциал фосфора в полной мере еще не реализован. Это предположение выдвигается потому что он играет огромную роль в организме человека. В частности уже известно, что фосфор является составной частью цепей РНК и ДНК. На сегодняшний день ведуться исследования по воздействию на эти цепи. Вы только представьте, что в один прекрасный день можно будет избавиться от всех страшных болезней путем воздействия на цепь ДНК человека. Среднестатистический взрослый человек имеет около 700 грамм фосфора в составе своего организма. Большая его часть содержится в костях и зубах в виде аппатита. Недостаток фосфора в организме может пагубно влиять на здоровье человека.
Стоит отметить еще высокую токсичность этого элемента. Вернее не его самого, а именно его аллотропов. В пример можно привести белый фосфор. Раньше использование белого фосфора было очень широко. Чтобы было понятней его использовали даже в спичках, вместо привычной нам сегодня серы. От него пришлось отказаться из-за его высокой токсичности. Так же он имеет возможность самовоспламеняться. Температура самовоспламенения его пыли составляет 34°C, что очень приближено к комнатной. Поэтому он представляет опасность со всевозможных сторон безопасности.
















Очень интересно. Замечательная статья